«Стадион ЦСКА практически готов к открытию. Реконструкция «Лужников» идет с...

Мышечная спастичность - это нарушение, о котором редко подробно рассказывают людям, перенесшим инсульт. Клиницисты склонны описывать мышечную спастичность с точки зрения ее влияния на конечности. Например, они могут сказать: «Инсульт вызывает напряжение в руке» или «Ваши мышцы напрягаются из-за поражения мозга вследствие инсульта». Это неполные объяснения мышечной спастичности. Вам нужно знать всю правду. Без понимания причин мышечной спастичности у вас мало шансов ее ослабить. Большая часть восстановления после инсульта, в том числе уменьшение мышечной спастичности, идет изнутри. Только сам человек, перенесший инсульт, может уменьшить мышечную спастичность. Как и в случае многих других аспектов реабилитации после инсульта, человек «ведет свою нервную систему» к восстановлению. Мышечная спастичность - проблема нервной системы, вызванная недостаточным контролем мозга над мышцами. Мышцы поражены, но причина не в них.
Как можно уменьшить или устранить мышечную спастичность без лекарств или хирургической операции? Единственный способ ослабить ее состоит в том, чтобы восстановить контроль мозга над спастическими мышцами. Использование нейропластического процесса - единственный способ восстановить контроль над мышцами. Понимание мышечной спастичности поможет вам использовать нейропластический процесс для ее уменьшения.
Вот научно обоснованное и, будем надеяться, понятное объяснение мышечной спастичности.
Ваши мышцы посылают постоянные сообщения в мозг о степени напряжения, испытываемого ими. Если мышцы будут слишком напряжены, то они порвутся. Мозг находится в постоянном взаимодействии с мышцами, чтобы удостовериться, что мышца помогает вам двигаться и ей не угрожает разрыв.
Ваш мозг приказывает мышцам, когда сокращаться (напрягаться, чтобы помочь вам двигаться) и когда расслабляться.
Если ваш мозг не способен в полной мере управлять мышцами, что заставляет их напрягаться? Действуют ли мышцы самостоятельно? Или что-то приказывает им сокращаться?
Импульс, который посылает спинной мозг, чтобы защитить мышцы, подобен рефлексу растяжения. Такой рефлекс возникает, например, при проверке врачом рефлексов неврологическим молоточком. Когда врач ударяет вас чуть ниже коленной чашечки, нога выпрямляется в колене, независимо от того, хотите вы этого или нет. Движение ноги, резко поднимающейся вперед, называют рефлексом растяжения. Рефлексы растяжения предотвращают разрыв мышц, мгновенно сокращая мышцы. Представьте, если бы врач постоянно ударял по колену, не останавливаясь. Мышечную спастичность можно рассматривать подобным образом. Иными словами, мышечная спастичность - это многократное действие рефлексов.
И это повторяется снова и снова: мышцы все время кричат: «Помогите!» - а спинной мозг приказывает: «Сокращайтесь!» Этот процесс заставляет мышцу напрягаться сильнее, что приводит к еще большему количеству сигналов о помощи от мышцы. У некоторых перенесших инсульт мышечная спастичность может сохраняться всегда, кроме самых глубоких стадий сна. Однако у большинства людей, переживших инсульт, мышечная спастичность уменьшается перед засыпанием.
Мозг использует мышцы, чтобы управлять движениями. Мышцы будут сокращаться и расслабятся так, чтобы вы могли плавно двигаться. После инсульта связь между мозгом и мышцами на больной стороне разрывается. Контроль над мышцами поврежденной стороны может ослабнуть (или исчезнуть), а мышцы не любят, когда их не контролируют. Так как мышцы больше не контролируются, они обращаются к спинному мозгу. Именно эти отношения между мышцами и спинным мозгом лежат в основе мышечной спастичности. После инсульта мозг больше не способен защищать мышцы от чрезмерного растягивания и разрыва, поэтому спинной мозг берет эти обязанности на себя и приказывает мышцам оставаться напряженными, что и защищает их от разрыва. Мышечная спастичность - это защитный механизм. Конечно, напряженные мышцы мешают двигаться. Никакие лекарственные препараты, методы лечения или способы терапевтического воздействия не устранят мышечную спастичность. Все они дают временный эффект; как только такое лечение прекращается, мышечная спастичность возвращается. Однако надежда остается. Очевидный ответ на эту загадку прост: периодически приводите спастические мышцы в движение.
Мышцы избавляются от спастичности с помощью нашего старого друга - нейропластичности. Инсульт убивает часть мозга, которая управляет спастическими мышцами. Но что, если бы все было наоборот? Что, если бы вы могли задействовать больше мозга для контроля спастических мышц? Это и есть нейропластическая модель уменьшения мышечной спастичности. Идея состоит в том, чтобы использовать методы, позволяющие передать контроль над спастическими мышцами другим областям мозга. Когда мозг восстанавливает контроль над мышцами, спастичность ослабевает. Напряженность мышц становится менее интенсивной, что, в свою очередь, обеспечивает больший контроль движений, а это дает возможность увеличить амплитуду движений. Более широкая амплитуда движений позволяет телу стимулировать еще больше изменений в мозге. Чем лучше мозг контролирует мышцы, тем больше доступно движений. Чем больше доступно движений, тем сильнее можно стимулировать изменения в мозге и т. д.
Основной способ восстановления контроля мозга над спастическими мышцами - повторяющаяся практика. Например, терапия вынужденными движениями, которая требует большого количества повторяющейся практики, часто позволяет уменьшить мышечную спастичность. Но при использовании любой стандартной «терапии» или «схемы лечения» от вас не требуется никаких усилий для восстановления контроля мозга над спастическими мышцами. Чтобы заставить мозг взять на себя ответственность за мышцы, требуется многократное (повторяющееся) использование этих мышц. Эти повторяющиеся усилия также должны быть трудными - «на пределе» ваших текущих возможностей.
Проще говоря, многократные и сложные тренировки спастических мышц уменьшают мышечную спастичность, потому что:
Нисходящая спираль после инсульта
Инсульт. -> Часть мозга, управляющая мышцами, поражена. -> Мозг не может ни управлять мышцами, ни защищать их. -> Спинной мозг защищает мышцы, заставляя их напрягаться. -> Мышцы укорачиваются навсегда. -> Напряженные, укороченные мышцы еще больше затрудняют движения.
Повторяющаяся практика перестраивает мозг. -» Мозг восстанавливает контроль над мышцами. -> Спинной мозг передает контроль над мышцами головному мозгу. -> Мышечная спастичность уменьшается или исчезает. -» Движения становятся более нормальными.
Единственный способ навсегда уменьшить или устранить мышечную спастичность - перестроить мозг, чтобы восстановить контроль над мышцами. Мышечную спастичность будут уменьшать те же варианты восстановления, которые вызывают перестройку мозга. Улучшение движений и уменьшение спастичности - это две стороны одной монеты.
Исследования на животных показали, что, если конечность обездвижена (обычно путем ее привязывания к телу), количество клеток головного мозга, отвечающих за эту конечность, уменьшается. Именно это происходит с людьми, перенесшими инсульт, у которых отмечается мышечная спастичность: их мышцы обездвижены. Если спастические мышцы снова начинают двигаться, то часть мозга, отвечающая за эти мышцы, становится больше. По мере того как все больше нейронов оказываются способными контролировать эти мышцы, мышечная спастичность уменьшается.
Методы лечения, используемые физиотерапевтами и невропатологами, помогут вам перестроить мозг, чтобы восстановить контроль над спастическими мышцами. Эти врачи специально обучены способам терапии, которые уменьшают мышечную спастичность. Лечение некоторыми лекарственными средствами и другие методы терапии обеспечивают временное ослабление мышечной спастичности. Это временное улучшение состояния может облегчить движения. Оно также помогает создать возможность для тяжелой работы по перестройке мозга.
Лекарственные препараты, используемые для уменьшения мышечной спастичности, относятся к двум следующим группам:
Такие препараты могут уменьшить мышечную спастичность, что будет способствовать:
Спросите своего врача об этих вариантах. Но помните, что эти лекарства не устраняют первопричину мышечной спастичности (недостаточный контроль мозга над мышцами). Никакое лекарственное средство не заменит тяжелой работы, необходимой для перестройки мозга. Лекарственные препараты и другое лечение, которое временно уменьшает мышечную спастичность, дают вам возможность заниматься напряженной работой по перестройке мозга.
Эта работа может проводиться в форме:
Этот список будет расширяться с появлением результатов новых исследований, поэтому продолжайте подбирать методы лечения и задавайте больше вопросов.
Консультации с врачами, терапевтами и другими медработниками помогут направить ваше лечение так, чтобы достичь уменьшения мышечной спастичности с минимумом затрат и максимумом лечебного эффекта.
Вы с врачом можете решить использовать лекарства от мышечной спастичности не только для облегчения нейропластических изменений. Имеются и другие серьезные основания для назначения пероральных и других лекарственных препаратов от мышечной спастичности. Целью длительного использования системного лекарственного лечения может быть увеличение подвижности, уменьшение боли, улучшение движений и т. д.
В некоторой степени мышечная спастичность может быть временно полезна в конце «вялой фазы» восстановления.
Сразу после инсульта некоторые пациенты испытывают вялость (слабость) мышц на пораженной стороне. Человек, перенесший инсульт, ничем не может двигать самостоятельно на поврежденной стороне. Это ужасное время для переживших инсульт и их семей. Есть злая шутка в том, что люди находятся в таком плохом состоянии сразу после инсульта, когда они меньше всего могут понять, что произошло, и реагировать на это.
Исследования показывают, что люди, у которых вялость мышц сохраняется в течение года после инсульта, могут надеяться лишь на ограниченное восстановление. Но у некоторых больных, отмечающих у себя вялость мышц, в действительности ее нет. Отчасти проблема заключается в терминах, используемых для описания нарушения движений. Часто слово «парализованный» употребляется вместо слова «гемипаретический». Гемипарез предполагает наличие слабости на одной стороне тела, а не паралича. Есть только два вида истинного паралича после инсульта:
Эти формы паралича встречаются редко. Большинство перенесших инсульт относятся к общей категории «гемипарети-ческие».
Некоторые люди думают, что это различие не имеет значения, но они неправы. Небольшие движения могут использоваться в качестве отправного пункта для овладения гораздо лучшими и более скоординированными движениями. Поэтому есть огромная разница между «отсутствием движения» и «небольшими движениями». Если у человека вялость мышц сохраняется в течение года, то прогноз на восстановление движений неблагоприятный. Когда у пациента есть небольшие движения, это означает, что у него сохранились связи между головным мозгом и мышцами, и наращивание этих связей свидетельствует о наличии потенциала для улучшения движений.
Стадии восстановления после инсульта, описанные Бруннстрём , показывают, что, когда люди выздоравливают, они начинают с фазы вялости и затем вступают в этап спастичности мышц. Наличие мышечной спастичности рассматривается как период надежды, потому что способность мышц сокращаться наконец возобновляется. С появлением мышечной спастичности часто отмечаются небольшие синергичные движения .
В соответствии со стадиями, предложенными Бруннстрём, после периода вялости появляется мышечная спастичность. Можно ли рассматривать мышечную спастичность в каком-то положительном свете? На самом деле есть негативные и позитивные аспекты этого явления.
Мышечная спастичность вредна, потому что она:
Мышечая спастичность полезна тем, что:
Появление мышечной спастичности можно рассматривать как положительный знак на пути к восстановлению. Но как только мышечная спастичность возникает, следующая стадия восстановления требует ее сокращения и возможного устранения. Как верно для большей части процесса восстановления после инсульта, пока делается одна работа, уже начинается другая.
Медработники и люди, перенесшие инсульт, иногда ошибаются, думая, что мышечная спастичность в руке - это проблема с рукой или что мышечная спастичность в ноге - это проблема с ногой. Очевидно одно: мышечная спастичность - это проблема с мозгом. Мышечная спастичность - это симптом поражения головного мозга, вызванного инсультом. Мышечная спастичность - это защитный механизм, который не позволяет мышцам рваться. Головной мозг больше не выполняет своих функций, поэтому спинной мозг берет на себя работу по защите мышц, суставов и других мягких тканей (то есть нервов, кровеносных сосудов и самих мышц). Спинной мозг раз за разом отправляет всего одно сообщение: «Мышцы, защитите себя! Напрягитесь!»
Многие исследователи полагают, что если мозг в достаточной степени проявит нейропластичность (перестроится), то мышечная спастичность уменьшится. Но здесь есть одна проблема. Чтобы начался нейропластический процесс, вы должны обладать способностью инициировать движения. Если мышечная спастичность слишком сильна, движения становятся невозможными. Если для нейропластичности нужны какие-то движения, но конечности и пальцы человека, перенесшего инсульт, не двигаются из-за мышечной спастичности, то как вам запустить данный процесс? Некоторым людям, перенесшим инсульт, может помочь следующий способ.
Есть три лекарственных препарата, которые можно использовать для воздействия на определенные спастические мышцы: ботокс, фенол и алкоголь. Этот метод лечения называют «блокадой нервов». Обычно он применяется физиотерапевтами или невропатологами.
Ботокс получил известность в основном как средство избавления от морщин. Способ, которым он устраняет морщины, важен для понимания того, как препарат действует на спастические мышцы. Складки на лице создаются и увеличиваются мышцами, отвечающими за движения лица, когда вы хмуритесь, щуритесь и морщите лоб. Врач может ввести ботокс, который временно парализует эти мышцы и заставляет их меньше стягивать лицо, сокращая количество морщин. Ботокс действует на спастические мышцы таким же образом: он их расслабляет.
Если вы, слыша слово «ботулизм», сразу думаете о пищевом отравлении, при котором людям становится плохо из-за испорченной еды, то вы правы. Ботокс производится из тех же бактерий, которые вызывают ботулизм. Бактерии Clostridium botulinum выделяют вещество, способное парализовать мышцы. Его собирают и делают из него ботокс. Данный препарат не содержит бактерий, которые вызывают ботулизм, и не заражает пациентов ботулизмом. Ботокс уменьшает выработку ацетилхолина - химического вещества, которое позволяет нервному импульсу достигать мышц. Таким образом, он блокирует нервные импульсы, вызывающие мышечную спастичность.
Эти препараты вводятся непосредственно в спастические мышцы. Как и ботокс, они временно расслабляют их, таким образом уменьшая мышечную спастичность. Эти средства довольно часто использовались до появления ботокса. Следует отметить, что антиспастические препараты для блокады нервов на основе фенола и алкоголя значительно дешевле, чем ботокс.
Сочетание блокады нервов и тренировок для стимулирования движений может быть эффективным для улучшения движений и устойчивого уменьшения мышечной спастичности. Ботокс вводится в напряженные мышцы, затем эти мышцы расслабляются достаточно для того, чтобы обнаружить имеющиеся движения. Идея состоит в том, чтобы сделать возможными варианты восстановления, способствующие перестройке мозга, используя движения, которые были недоступны до блокады нервов. Любое лечение мышц с помощью блокады нервов обычно расслабляет их на несколько месяцев. Такая терапия позволяет увеличить активные (выполняемые самостоятельно) движения. Однако в некоторых случаях блокаду нервов можно применять многократно, каждый раз создавая возможность для улучшения движений.
Есть сочетание методов лечения, которое при правильном использовании может запустить процесс уменьшения мышечной спастичности и стимулировать движения. Это сочетание состоит из трех частей:
Пример А
Роберт не может поднять пораженную стопу, потому что у него сильная спастичность в мышцах, которые ее опускают (икроножных). Он идет к врачу. Врач направляет Роберта к физиотерапевту.
Пример Б
У Кэти кисть всегда согнута в запястье, а пальцы сжаты. Мышечная спастичность заставляет ее все время держать руку сжатой в кулак, поэтому ногти врезаются в ладонь. Это приводит к порезам на ладони Кэти и затрудняет мытье руки. Кэти идет к невропатологу.
Некоторые врачи делают инъекции для блокады нервов, но допускают ошибку, отказываясь от каких-либо вмешательств, основанных на расслаблении мышц в результате блокады нервов. Блокада нервов не устраняет мышечную спастичность навсегда. Вместо этого она создает возможности для устойчивого уменьшения мышечной спастичности. После терапии с помощью блокады нервов необходимо какое-то вмешательство для использования возможностей, созданных этим лечением.
Короткое замечание о ботоксе: некоторые исследования показали, что электростимуляция мышц, в которые был введен ботокс, может дать два преимущества.
Таким образом, прямая избирательная стимуляция целевых мышц уменьшит количество необходимого ботокса и повысит эффективность данного препарата. Это лечение должен одобрить ваш лечащий врач.
Вот неполный список методов лечения, которые могут быть эффективными в сочетании с блокадой нервов:
Есть еще два варианта лечения для людей с мышечной спастичностью. Один из них воздействует непосредственно на мышечную спастичность, а другой - на симптомы мышечной спастичности.
Ботокс назначают врачи, обычно физиотерапевты или невропатологи. Врач решит, нужно ли вам лечение этим препаратом. После применения ботокса можно использовать дополнительную терапию, чтобы стимулировать расслабление мышц, вызванное действием этого препарата. Варианты восстановления, включающие электростимуляцию, имеют противопоказания и применяются с соблюдением мер предосторожности. Обсудите их со своим лечащим врачом.
Снять спастику после инсульта оказалось чрезвычайно трудно. Дело в возникающем противоречии. Мы упёрто восстанавливали силу и выносливость. Делали это с помощью специальных упражнений с высокой нагрузкой и кучей повторений.
Для лечения спастики это помеха и вред. При снятии спастики нужен расслабляющий массаж и легкие движения в упражнениях. Что бы продолжить восстановление после инсульта надо проводить взаимоисключающие занятия. Но мы придумали простое решение. Сделать две группы занятий.
Первая: для восстановления силы и выносливости. Вторая для лечения спастики, восстановления равновесия и координации. Решение оказалось очень правильным. Правда мы допёрли до него не сразу и некоторое время делали упражнения для снятия спастики вместе с упражнениями на силу и выносливость. Вовремя заметили, что от активных упражнений спастика усиливается.
Проявляется спастика в скованности. Невозможно сделать быстрое или резкое движение. Постоянно напряженные мышцы блокируют свободу
. Чувство словно ты сильно заржавевший Терминатор))).
Напряжение приводит к скорой утомляемости.
Восстановление после инсульта может быть фактически заблокировано спастикой. Трудно восстанавливать навыки, когда конечности словно связаны резинками и всегда находятся в напряженном, неестественном положении. Для снятия спастики после инсульта мы применяем элементарные упражнения. Главное делать их легко, без напряжения.
Спастика мышц — это непроизвольное их сокращение, судороги или спазм вследствие нарушения проводимости нервных импульсов после травмы спинного и головного мозга.
Чаще это состояние проявляется ночью, но так же может существенно затруднить жизнь днем.
Основной причиной формирования судорог специалисты называют дисбаланс тормозного влияния двигательных элементов коры головного на клетки в структуре спинного мозга.
Закономерным итогом становится растормаживание тонического рефлекса – формируется мышечная спастика в пораженных травмой конечностях человека.
В нормальном состоянии человеку не приходиться задумываться об очередности производимых в мышцах явлениях: какие из них сначала требуется сократить, затем расслабить – наш мозг довел подобную деятельность до автоматизма.
После инсульта или травмы происходит гибель клеточных элементов, несущих ответственность за специальные тормозящие импульсы в двигательных нейронах головного и спинного мозга. Рефлекторная дуга: конечность – спинной мозг – головной мозг перестает быть единой системой – происходит нарушение координации.
Спазмы формируются далеко не сразу – на протяжении недель , и даже месяцев. Приводит к значительным вторичным изменениям в мышцах и суставах – усиливает отрицательное воздействие парезов на двигательную систему.
Первые признаки начала формирования спастики мышц наблюдаются в первые же сутки после травмы, а в последующем имеют тенденцию к усилению.
Изменяться степень выраженности может под неблагоприятным воздействием негативных факторов, к примеру:
При усилении интенсивности нагрузки на мышечные волокна в конечностях, происходит затруднение их двигательной активности, наблюдаются симптомы болевых ощущений в них, различной степени выраженности.
По степени выраженности спастики различают следующие формы:

Спастика ног в легкой форме проявляется быстрой утомляемостью мышц голеней, ощущение «забитости мышц», от физической деятельности, ходить при этом легче становится на каблуке, затем становится затруднительно потянуть к себе пальцы ног и разогнуть ее в колене.
В тяжелой форме спазма: одна или две ноги фиксируются в согнутом в коленном или тазобедренном суставах, а стопа выворачивается внутрь или наружу. При хождении без специальной обуви или , могут возникнуть деформации или контрактуры.
Проявление спастике рук в легкой форме: затруднено разгибание
пальцев и выпрямление руки в локтевом суставе, признаком тяжелой формы является согнутые в локтевом и плечевом суставах, кисть при этом сжата в кулак.
Если спастика присутствует долгое время без лечения, развивается контрактура, то есть сустав фиксируется не в физиологическом для организма состоянии.
В дальнейшем же, спазм будет иметь лишь отрицательное влияние на проведение восстановительных мероприятий. Помимо конечностей, будет ухудшать восстановление и в позвоночнике: повышение тонуса мышц вызывает болевые ощущения в спине – симптомы вертеброгенного радикулита.
Специалисты отмечают: чем раньше было начато адекватное лечение современными препаратами, а также, чем меньше выраженность спастики– тем лучше будет прогноз реабилитационных мероприятий.
Даже, если симптомы значительно выражены, а лечение судорог в силу определенных причин начались в более поздний временной промежуток – уменьшение спастики существенно улучшает общее самочувствие.
Наиболее важным требованием, предъявляемым к лечению, является его максимально возможная безболезненность, поскольку боль многократно усиливается спастикой.
Важным моментом является и контроль за деятельностью тазовых органов – предупреждение воспалительных проявлений в них, а также своевременно проводить мероприятия по предупреждению возникновения контрактур и .
 Комплекс современного лечения по избавлению от спастики:
Комплекс современного лечения по избавлению от спастики:
Комплекс лечения подбирается только индивидуально, в прямой зависимости от локализации очага и степени выраженности спастики. Необходимо учитывать и технические возможности медицинского учреждения.
Спастика после инсульта или травмы головного мозга обязательно требует медикаментозного воздействия. Лечение должно проводиться поэтапно – с постепенным наращиванием лечебной дозы медикаментов, возможно заменой препарата.
 На сегодняшний день востребованы две подгруппы:
На сегодняшний день востребованы две подгруппы:
Как и у иных подгрупп даже самых современных препаратов, у вышеперечисленных имеют свои противопоказания, поэтому их назначением должен заниматься только высококвалифицированный специалист невролог.
Лечение спастики длительной укладкой конечностей человека, в такое положение, когда мышцы оптимально растянуты, а тоническая рефлекторная активность уменьшена, именуется специалистами ортезированием. Оно способствует снижению гипертонуса в конечностях – патологические симптомы удается многократно уменьшить.
При выраженной спастике рекомендуется даже наложение специальной гипсовой лангеты либо шины – для предотвращения развития контрактуры. Именно шина фиксирует конечность в наиболее приемлемом положении — при котором мышечные волокна располагаются в растянутом положении.
Лечение ортезированием проводится от одного до двух часов, в прямой зависимости от ощущений человека – при усилении болевых ощущений, процедуру заканчивают.
 Лечение с помощью упражнений, направленных на оптимальное расслабление волокон в мышцах – давно проверенный, успевший себя отлично зарекомендовать реабилитационный прием лечения спастики.
Лечение с помощью упражнений, направленных на оптимальное расслабление волокон в мышцах – давно проверенный, успевший себя отлично зарекомендовать реабилитационный прием лечения спастики.
Дозированное лечебное растягивание позволяет на пару часов понизить их тонус, максимально увеличить объем движений в пораженных конечностях.
Кинезиотерапевт знает, что снижение тонуса будет наблюдаться лишь определенное время а потому его необходимо эффективно использовать для проведения иных комплексных упражнений, которые были затруднены из-за спастики.
Хирургическое вмешательство определяется специалистом по строго индивидуальным показаниям, когда консервативные методики уже исчерпали себя, а выраженной положительной динамики не наблюдается.
Снять спастику задача важная. Она сильно мешает в повседневной жизни, отнимает силы и сковывает движения. Это мешает восстанавливать утраченные навыки и выносливость. Чтобы полноценно проводить восстановление после инсульта, нужно обязательно вылечить спастику. Мы это выполняем параллельно с остальными задачами.
При комплексном подходе и начале лечебных мероприятий на возможно более раннем этапе, медикаментозного лечения – нормализация мышечного тонуса способствует максимальному ускорению восстановления больного.
В лечении хорошо себя показали такие методы как, миостимуляция,ботокс, конечно лечебная гимнастика, медицинские препараты(мидокалм, баклофен) и щадящая хирургия.
Что такое, причины возникновения спастичности, недопущение и лечение обновлено: Ноябрь 21, 2017 автором: автор
Для цитирования:
Дамулин И.В. Спастичность после инсульта // РМЖ. 2005. №7. С. 501
Инсульт остается крайне важной медико–социальной проблемой, поскольку является одной из наиболее частых причин инвалидизации, в большинстве случаев связанной с двигательными нарушениями . У 80–90% больных в остром периоде инсульта выявляется гемипарез, остаточные явления перенесенного инсульта различной степени выраженности и характера отмечаются примерно у 2/3 больных. Почти 3/4 лиц с инсультом – в возрасте 65 лет и старше, при этом частота инсульта примерно на 20% выше у мужчин, чем у женщин.
Более чем у 50% пациентов имеется артериальная гипертензия, у 25% – сахарный диабет, почти у 25% – указание в анамнезе на перенесенный в прошлом инсульт. Помимо артериальной гипертензии и сахарного диабета, факторами риска развития инсульта являются поражения магистральных сосудов головного мозга, фибрилляция предсердий, курение, гиперлипидемия и повышенный уровень фибриногена. У лиц молодого возраста среди основных факторов риска развития инсульта следует отметить церебральные эмболии, травму экстракраниальных сосудов, васкулопатии различного генеза, нарушения коагулогических свойств крови, использование оральных контрацептивных препаратов, роды, наркоманию (особенно кокаиновую зависимость), а также заболевания, связанные с ВИЧ–инфицированием. Следует заметить, что кокаин приводит к цереброваскулярным нарушениям, воздействуя на артериальное давление и тонус сосудов, вызывая длительный вазоспазм, увеличивая синтез тромбоксана и повышая склонность тромбоцитов к тромбообразованию, при этом также увеличивается риск возникновения кардиогенных эмболий . Хроническое употребление кокаина приводит к церебральной атрофии и патологии белого вещества полушарий головного мозга . По данным методов функциональной нейровизуализации выявляются множественные зоны церебральной гипоперфузии . Довольно характерны для этой категории больных нарушения лобного типа, проявляющиеся, в частности, увеличением числа ошибок персеверативного типа при выполнении Висконсинского теста сортировки карточек . Васкулиты являются причиной лишь 3–5% инсультов у лиц моложе 50 лет . Заболеваемость церебральными васкулитами составляет 1–2 случая на 1 млн населения в год (для сравнения: системными васкулитами – 39 случаев) . Основным механизмом, приводящим к поражению нервной системы при васкулитах, является ишемия . Возникновение ишемии при воспалении стенки сосудов связано с тремя патогенетическими факторами: обструкцией сосудов, увеличением склонности к коагуляции крови, что обусловлено влиянием провоспалительных цитокинов на поверхность эндотелия и изменением сосудистого тонуса . Однако чаще при васкулитах поражаются сосуды висцеральных органов или сосуды, кровоснабжающие периферические нервы . Возможно, это обусловлено особенностями строения стенки церебральных сосудов (в частности, лимфоцитарная адгезия эндотелия церебральных сосудов меньше 5%, в других органах – 15–20%) и наличием гематоэнцефалического барьера .
Одним из серьезных осложнений перенесенного инсульта является спастичность в пораженных конечностях, которая отмечается почти у 65% больных, перенесших инсульт. У больных со спастичностью существенно возрастает риск падений и, соответственно, травматизации, нередко возникают контрактуры, болевые синдромы, пролежни, остеопороз, тазовые расстройства и тромбофлебиты. Непосредственной причиной летального исхода этой категории больных могут быть сердечно–сосудистые, легочные или почечные осложнения.
Под спастичностью понимается двигательное расстройство, которое характеризуется скорость–зависимым повышением тонических рефлексов растяжения в результате поражения верхнего мотонейрона . Клинически это проявляется повышенным мышечным сопротивлением, варьирующим по своей выраженности в зависимости от амплитуды и угловой скорости производимого пассивного движения. Характерным для спастичности признаком является феномен «складного ножа», когда при пассивном сгибании пораженной конечности выраженное в начале движения сопротивление мышцы внезапно сменяется ее сокращением в направлении производимого движения. Спастичность, как правило, сопровождается парезом и иной симптоматикой, характерной для поражения верхнего мотонейрона. Среди клинических признаков поражения верхнего мотонейрона выделяют т.н. «позитивные» и «негативные» симптомы, а также изменения спастически сокращенных мышц (табл. 1).
Сразу после развития инсульта мышечный тонус в паретичных конечностях чаще снижен, однако в течение 2–3 дней он повышается, приводя, в конечном счете, к характерной позе с повышением тонуса в аддукторах и флексорах руки и аддукторах и экстензорах ноги. Легкие изменения в двигательной сфере в виде некоторого снижения мышечной силы и оживления рефлексов могут отмечаться и на ипсилатеральной стороне. Повышение мышечного тонуса в паретичных конечностях может возникать не только по прошествии нескольких дней от начала заболевания, но и спустя более продолжительный период времени (через недели и даже месяцы) .
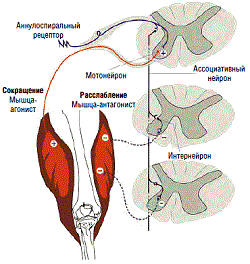
Выраженность клинических проявлений может варьировать в зависимости от локализации очага, объема пораженной ткани и длительности заболевания. Регуляция мышечного тонуса осуществляется под влиянием как центральной, так и периферической импульсации на a–мотонейроны спинного мозга. a–мотонейроны, которые иннервируют мышечные волокна, располагаются в области передних рогов спинного мозга. Афферентные импульсы от рецепторов в мышцах передаются к структурам спинного мозга по сенсорным волокнам. Сенсорные волокна заканчиваются на a–мотонейронах передних рогов (моносинаптические пути), а также на вставочных нейронах задних рогов спинного мозга, связанных, в свою очередь, с двигательными нейронами, иннервирующими мышцы–антагонисты (полисинаптические пути). В основе возникновения спастичности лежит нарушение тормозящих влияний супраспинальных отделов на спинальные двигательные и вставочные нейроны. При этом на спинальном уровне возникает нарушение баланса между процессами возбуждения и торможения, а также денервационная гиперчувствительность и нейрональный спраутинг. Высказывавшееся ранее предположение о селективной гиперактивности g–системы, как одном из ведущих патогенетических механизмов спастичности, достоверных экспериментальных подтверждений не нашло.
При длительно существующем пирамидном синдроме определенное влияние на повышение мышечного тонуса оказывают также изменения самих мышц (табл. 2).
Ряд из этих расстройств (изменение реакции на растяжение, нарушение быстрого расслабления мышечного волокна, нарушение реципрокного ингибирования, нарушение сократительных способностей мышцы вследствие изменения структуры мышечного волокна, вторичное возникновение боли и нарушение способности мышц–антагонистов оказывать сопротивление, сопоставимое с действием спастически измененных мышц) могут быть уменьшены при использовании методов хемоденервации мышц или введении препаратов ботулинического токсина. Однако снижение мышечной силы и увеличение латентного периода активации мышцы при подобном лечении могут нарастать .
Несмотря на то, что спастичность считается одним из характерных признаков поражения кортикоспинального пути, в основе ее возникновения лежит поражение экстрапирамидных двигательных путей. Важную роль в регуляции мышечного тонуса играют ретикулоспинальные и вестибулоспинальные нисходящие пути. Само по себе изолированное поражение пирамидных путей на уровне коры, ножек мозга, основания моста или пирамид продолговатого мозга не сопровождается повышением мышечного тонуса .
В реабилитационном периоде после инсульта вначале происходит восстановление движений в проксимальных отделах конечностей, затем – в дистальных. Обычно при инсульте соответствующей локализации слабость в верхних конечностях возникает раньше, чем слабость в нижних конечностях, и, как правило, восстановление нормальных двигательных функций в гемипаретичной руке происходит хуже, чем в ноге. Одним из объяснений этому является то, что функциональное восстановление в руке включает не только регресс мышечной слабости, но также восстановление способности к выполнению тонких скоординированных движений. В отличие от этого функциональное восстановление в ноге, что проявляется восстановлением ходьбы, может протекать даже при незначительном или умеренном нарастании мышечной силы. Кроме того, успех реабилитационных мероприятий в руке может быть в значительной мере ограничен из–за присоединения изменений в плечевом суставе и связанном с этим возникновением боли.
Существенно хуже прогноз восстановления двигательных функций в руке, если плегия отмечается сразу в начале заболевания, а также в случае, если через 4 недели от начала заболевания не происходит восстановления хватания рукой. Однако примерно у 9% больных с выраженным парезом в руке в остром периоде заболевания в последующем можно добиться удовлетворительного восстановления, а у 70% пациентов, у которых отмечается некоторое улучшение двигательных функций в течение первых 4 недель от начала заболевания, в последующем отмечается полное или значительное восстановление двигательных функций в руке. Считается, что если у пациента в течение первых 2 недель от начала инсульта отсутствуют активные движения в конечностях, то в дальнейшем полного регресса двигательных расстройств не будет . В случае самостоятельного полного восстановления утраченных двигательных функций длительность периода восстановления, как правило, не превышает 3 месяцев (обычно 1,5–2 месяца после инсульта), однако в ряде случаев некоторое улучшение может продолжаться до 6–12 месяцев и даже более длительный период времени.
Спастичность приводит к существенным функциональным расстройствам и нарушению качества жизни больных. Однако сама по себе спастичность не всегда требует лечения, а уменьшение повышенного мышечного тонуса не во всех случаях имеет позитивное значение для больного . Например, у ряда пациентов с выраженными парезами наличие спастичности в мышцах, анатомически и функционально препятствующих силе тяжести («антигравитационные» мышцы), может облегчать стояние и ходьбу. Кроме того, наличие повышенного мышечного тонуса может препятствовать развитию мышечных атрофий, отека мягких тканей и остеопороза, а также уменьшать риск развития тромбоза глубоких вен нижних конечностей. Показаниями для лечения спастичности являются лишь те случаи, когда вследствие повышенного тонуса мышц нарушается «функционирование, позиционирование или комфорт».
Основными задачами лечения являются не только уменьшение выраженности патологически повышенного тонуса мышц, но также снижение выраженности болевого синдрома, предотвращение развития контрактур, улучшение способности больного к самообслуживанию, облегчение проведения реабилитационных мероприятий. Поэтому, осматривая пациента со спастичностью, врач должен решить следующие задачи :
1. Выявить пациентов, являющихся кандидатами для проведения того или иного специфического метода антиспастической терапии.
2. Определить конкретный метод терапии, применение которого в плане восстановления двигательных функций может быть наиболее эффективным у данного больного (миорелаксанты, инъекции ботулинического токсина, местное введение фенола или алкоголя, дорсальная ризотомия).
3. Провести мониторинг динамики основных двигательных характеристик (мышечная сила, подвижность в суставах и т.д.) и функциональной активности больного (ходьба, способность к самообслуживанию, активность в обыденной жизни) на фоне терапии.
Таким образом, клиническая оценка спастичности должна проводиться не только с целью выявления пораженных мышц (или мышечных групп), но также для определения влияния существующей спастичности на все аспекты жизнедеятельности больного, включая способность к передвижению, трудоспособность и активность в повседневной жизни, что важно для планирования терапевтических программ (табл. 3). Для более детальной оценки может использоваться электромиография, а также диагностические локальные блокады с анестетиком, что помогает в выборе последующего метода лечения.
Оценивая повышение мышечного тонуса, следует учитывать и то, что он может существенно меняться в зависимости от позы больного и его эмоционального состояния . Усиление выраженности спастичности может происходить под влиянием внутренних факторов (при задержке мочеиспускания, воспалительных урологических заболеваниях, мочекаменной болезни, запорах) и внешних причин (переломы, неправильное положение спастической конечности в постели, тромбоз глубоких вен нижних конечностей).
Следует особо подчеркнуть, что спастичность клинически реализуется в различной форме и с участием разных механизмов, включая изменения как пресинаптического, так и постсинаптического торможения . Поэтому универсального, одинаково эффективного при всех вариантах спастического синдрома, метода лечения не существует. Однако поскольку в основе непосредственного повышения мышечного тонуса лежит патологическое усиление полисинаптических рефлексов и возбуждение спинальных мотонейронов, важным направлением медикаментозной терапии является воздействие на эти структуры .
При спастичности используются следующие методы лечения: физиотерапия и лечебная гимнастика, пероральный прием миорелаксантов, инъекции препаратов ботулинического токсина, интратекальное введение баклофена с помощью помпы, хемоденервация (фенол, алкоголизация), а также операции на сухожилиях, суставах и ризотомия. Первые три из них в настоящее время получили наиболее широкое распространение.
Физиотерапевтические методы и лечебная гимнастика наиболее эффективны в раннюю фазу возникновения спастичности и направлены на активацию естественных процессов восстановления. Ранее считалось, что одной из целей реабилитации больных, перенесших инсульт, является использование методик, в которых основной акцент делался на использовании непораженных конечностей с целью большей независимости пациентов в повседневной жизни. При этом на пораженные конечности сколько–нибудь значительная нагрузка не оказывалась. В настоящее время доказано, что активизация пораженных конечностей непосредственно влияет на процессы функциональной церебральной реорганизации и таким образом способствует лучшему восстановлению неврологического дефекта. Кроме того, чрезмерное использование больными с гемиплегией непораженных конечностей может привести к такому нежелательному явлению, как повышение тонуса в гемипаретичных конечностях . Широко используется лечение положением, тепловые и холодовые процедуры, фонофорез, чрескожная электростимуляция нервов и др. С помощью этих методик удается не только снизить повышенный мышечный тонус, но и увеличить объем движений в суставах, а также предотвратить возникновение контрактур. Все это в конечном итоге приводит к повышению функциональной активности больных. К сожалению, положительный эффект этих методов терапии, как правило, носит непродолжительный характер. К тому же до настоящего времени сколь–либо доказательные контролируемые исследования по изучению эффективности этих методик отсутствуют.
Использование препаратов ботулинического токсина более оправдано в ситуациях, когда мышечный спазм носит преимущественно локальный характер. Длительность эффекта определяется дозой введенного препарата, размером мышцы, активностью мышцы и еще рядом факторов, в том числе одновременным проведением физиотерапевтических процедур. Эффект от введения препарата сохраняется в среднем 2–6 мес. У некоторых больных может отмечаться исчезновение положительного эффекта после повторных инъекций ботулотоксина . Наиболее частыми причинами этого является неправильный выбор мышцы, в которую вводится препарат, или неадекватные дозы ботулотоксина. Однако у некоторых больных (менее 10%) может быть истинное отсутствие эффекта. Считается, что в основе этого может лежать блокирование антителами ботулотоксина типа А, однако результаты иммунологических методов исследования противоречивы . Следует заметить, что использование препаратов ботулинического токсина в значительной мере ограничено из–за их высокой стоимости.
В практической деятельности наиболее широко используются миорелаксанты – баклофен, тизанидин (Сирдалуд), диазепам, дантролен, толперизон . Среди препаратов этой группы Сирдалуд занимает особое место, что связано с механизмом его действия и клиническим эффектом. Являясь центральным a2–адренергическим агонистом, Сирдалуд обладает стимулирующим действием на моноаминергические ядра ствола головного мозга. Это приводит к торможению спинальных мотонейронов, связанных афферентными волокнами II типа со стволовыми центрами, и соответственно – к снижению мышечного тонуса. При этом уменьшается выброс возбуждающих аминокислот из вставочных спинальных нейронов. Нисходящие адренергические супраспинальные пути играют значительную роль в регуляции мышечного тонуса . Анатомически эти пути тесно связаны со спинальными структурами, особенно с передними рогами, результаты физиологических исследований свидетельствуют об их участии в регулировании рефлекторных спинальных ответов . В спинном мозге большая часть a2–рецепторов располагается на вставочных нейронах, а не на мотонейронах. Являясь производным клонидина, Сирдалуд обладает высоким сродством к a2– и практически не действует на a1–адренергические рецепторы . Под действием Сирдалуда происходит торможение высвобождения из спинальных нейронов аспартата . Этот препарат селективно ингибирует через a2–адренорецепторы вставочные нейроны задних рогов спинного мозга, что лежит в основе его анальгезирующего эффекта .
Высказывается предположение о том, что дополнительный антиспастический эффект Сирдалуда обусловлен его влиянием на a2–рецепторы норадренергических нейронов, располагающихся в области голубого пятна и оказывающих влияние на спинальные структуры . Было выявлено, что действие Сирдалуда, также как и норадреналина, на адренорецепторы не меняется на фоне введения a1– и b–адренергических антагонистов или антагониста опиатных рецепторов налоксона. В эксперименте не было выявлено действия Сирдалуда на клетки Рэншоу . D. Coward , анализируя результаты экспериментальных и клинических исследований, подчеркивает, что антиноцицептивный эффект Сирдалуда носит самостоятельный характер и не связан с его миорелаксирующим действием.
На фоне действия Сирдалуда снижается лишь тонический компонент мышечного сокращения при сохранности фазической реакции . Это отлично от действия баклофена, снижающего тонический и фазический компоненты, что сопровождается снижением силы мышц.
Таким образом, антиспастический эффект Сирдалуда связывают с несколькими механизмами действия (пресинаптическое и постсинаптическое ингибирование вставочных нейронов, возможное влияние на глутаматергическую систему). Существенным моментом является то, что Сирдалуд не противопоказан при наличии у пациентов эпилептических припадков, что делает возможным его назначение больным с постинсультными спастическими парезами и судорожными припадками. Экспериментальные данные свидетельствуют о возможном противоэпилептическом эффекте высоких доз препарата, механизм которого остается неясным . Однако в качестве собственно противоэпилептического препарата Сирдалуд не используется.
Антиспастический эффект Сирдалуда примерно сопоставим с эффектом баклофена и диазепама. Однако Сирдалуд имеет по сравнению с этими препаратами немаловажные преимущества – лучшую переносимость и отсутствие существенного снижения мышечной силы . Последнее обстоятельство существенно ограничивает использование баклофена и диазепама, поскольку снижение мышечной силы может отмечаться как в паретичных, так и в интактных конечностях. Следует заметить, что более 10% больных, начавших принимать баклофен, вынуждены в последующем отказаться от его приема из–за нарастания мышечной слабости.
Сирдалуд широко используется для лечения спастичности различного генеза . Положительный антиспастический эффект препарата носит дозозависимый характер, что подтверждается параллельным определением уровня препарата в плазме крови . Подбор индивидуально эффективной дозы (от 2 мг до максимальной дозы 36 мг/сут.) обычно осуществляется в течение 2–4 недель. После перорального приема действие препарата проявляется уже через 30–45 минут, максимальный эффект наступает в течение 1–2 часов . Улучшение отмечается у 60–82% больных (для сравнения: на фоне приема баклофена – у 60–65%, диазепама – у 60–83%), при этом спастичность снижается в среднем на 21–37% (на фоне приема плацебо – на 4–9%) .
Важно заметить, что механизм действия Сирдалуда существенно отличен от механизмов действия других препаратов, используемых для снижения повышенного мышечного тонуса. Поэтому Сирдалуд применяется в ситуациях, когда отсутствует антиспастический эффект других антиспастических средств (при так называемых «не отвечающих на лечение» случаях). Кроме того, учитывая различия в механизмах действия, Сирдалуд и баклофен могут использоваться для лечения спастичности в комбинации.
Для Сирдалуда характерен гастропротективный эффект, происхождение которого остается до конца не выясненным. Данные экспериментальных и клинических исследований свидетельствуют о его способности предохранять слизистую желудка от действия нестероидных противовоспалительных препаратов. Механизм этого эффекта связывают с адренергической активностью, торможением выработки желудочного секрета и способностью предотвращать изменения гликопротеинов, обусловленные влиянием аспирина или индометацина.
Частота возникновения таких побочных реакций, как головокружение, сонливость, сухость во рту, общая слабость, коррелирует с уровнем препарата в плазме крови . На фоне назначения Сирдалуда может отмечаться легкое снижение артериального давления , что объясняется структурным сходством этого препарата с клонидином . На здоровых добровольцах было показано, что на фоне разового приема 6–12 мг Сирдалуда снижение артериального давления составляет в среднем 10–15% . В литературе упоминается возможность Сирдалуда потенцировать действие гипотензивных препаратов .
В единичных случаях возможно преходящее увеличение уровня печеночных ферментов, исчезающее после уменьшения дозы или отмены препарата, поэтому следует осторожно назначать Сирдалуд пациентам с печеночной или почечной недостаточностью. Препарат, как правило, хорошо переносится и при длительных курсах терапии.
Литература
1. Ворлоу Ч.П., Денис М.С., Ван Гейн Ж. и др. Инсульт. Практическое руководство для ведения больных. –СПб.: Политехника, 1998. –629 с.
2. Гехт А.Б., Бурд Г.С., Селихова М.В. и соавт. Нарушения мышечного тонуса и их лечение сирдалудом у больных в раннем восстановительном периоде ишемического инсульта. //Журн. невролог. и психиатр. –1998. –Т.98, №10. –С.22–29
3. Гусев Е.И., Гехт А.Б. Спастичность. //Русск. мед. журн. –1999. –Т.7, №12. –С.567–571
4. Дамулин И.В. Постинсультные двигательные расстройства. //Consilium Medicum. –2003. –Т.5, №2. –С.64–70
5. Дамулин И.В. Принципы реабилитации пациентов, перенесших инсульт. //Справочник практического врача. –2003. –№2. –С.21–24
6. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. /В кн.: Болезни нервной системы. Руководство для врачей. Под ред. Н.Н.Яхно, Д.Р.Штульмана. Т.1. –М.: Медицина, 2001. –С.231–302
7. Кадыков А.С. Миорелаксанты при реабилитации больных с постинсультными двигательными нарушениями. //Журн. невролог. и психиатр. –1997. –Т.97, №9. –С.53–55
8. Окнин В.Ю. Баклофен в неврологической практике. //Лечение нервных болезней. –2002. –№3. –С.34–36
9. Парфенов В.А. Лечение больных, перенесших инсульт. //Русск. мед. журн. –2001. –Т.9, №7–8. –С.306–309
10. Салихов И.Г., Богданов Э.И., Заббарова А.Т., Васильева А.В. Принципы диагностики церебральных васкулитов. –Казань: КГМУ, 2001. –27 с.
11. Behari M. Spastisity. //Neurology India. –2002. –Vol.50. –P.235–237
12. Benecke R. Spasticity/Spasms: Clinical aspects and treatment. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.169–177
13. Benecke R. Botulinum toxin for spasms and spasticity in the lower extremities. //In: Therapy with Botulinum Toxin. Ed. by J.Jankovic, M.Hallet. –New York: Marcel Dekker, 1994. –P.557–565
14. Brin M.F. Botulinum toxin: chemistry, pharmacology, toxicity, and immunology. //Muscle & Nerve. –1997. –Vol.20, suppl.6. –P.S146–S168
15. Chen D.–F., Bianchetti M., Weisendanger M. Involvement of noradrenergic systems in the modulation of cutaneous reflexes. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.179–186
16. Coward D.M. Tizanidine: Neuropharmacology and mechanism of action. //Neurology. –1994. –Vol.44., N.11 (Suppl.9). –P.S6–S11
17. Davies J. Selective depression of synaptic transmission of spinal neurons in the cat by a new centrally acting muscle relaxant, 5–chloro–4–(2–imidazolin– 2–yl–amino)– 1,3–benzothiodazole (DS103–282). //Brit. J. Pharmacol. –1982. –Vol.76. –P.473–481
18. Davies J., Johnston S.E. Inhibition by DS 103–282 of D–(3–H)–aspartate release from spinal cord slices. //Brit. J. Pharmacol. –1983. –Vol.78. –P.28–30
19. Davies J., Johnston S.E. Selective antinociceptive effects of tizanidine (DS 103–282), a centrally acting muscle relaxant, on dorsal horn neurons in the feline spinal cord. //Brit. J. Pharmacol. –1984. –Vol.82. –P.409–421
20. Davies J., Quinlan J.E. Selective inhibition of responses of feline dorsal horn neurons to noxious cutaneous stimuli by tizanidine (DS103–282) and noradrenalin: Involvement of alfa2–adrenoceptors. //Neurosci. –1985. –Vol.16. –P.673–676
21. Delwaide P.J., Olivier E. Pathophysiological aspects of spasticity in man. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.153–167
22. Delwaide P.J., Pennisi G. Tizanidine and electrophysiologic analysis of spinal control mechanisms in humans with spasticity. //Neurology. –1994. –Vol.44., N.11 (Suppl.9). –P.S21–S28
23. Dietz V. Spastic movement disorder: what is the impact of research on clinical practice? //J. Neurol. Neurosurg. Psychiatry. –2003. –Vol.74. –P.820–821
24. Diez–Tejedor E., Frank A., Gutierrez M., Barreiro P. Encephalopathy and biopsy–proven cerebrovascular inflammatory changes in a cocaine abuser. //Eur. J. Neurol. –1998. –Vol.5. –P.103–107
25. Donaghy M. Toxic and environmental disorders of the nervous system. /In: Brain’s Diseases of the Nervous System. Tenth edition. Ed. by J.Walton. –Oxford etc.: Oxford University Press, 1993. –P.513–529
26. Enevoldson T.P. Recreational drugs and their neurological consequences. //J. Neurol. Neurosurg. Psychiatry. –2004. –Vol.75 (Suppl.3). –P.iii9–iii15
27. Filley C.M., Kleinschmidt–DeMasters B.K. Toxic leukoencephalopathy. //New Engl. J. Med. –2001. –Vol.345, N.6. –P. 425–432
28. Gormley M.E., O’Brien C.F., Yablon S.A. A clinical overview of treatment decisions in the management of spasticity. //Muscle & Nerve. –1997. –Vol.20, Suppl.6. –P.S14–S20
29. Gracies J.M., Nance P., Elovic E. et al. Traditional pharmacological treatments for spasticity. Part II: General and regional treatments. //Muscle & Nerve. –1997. –Vol.6 (Suppl.). –P.S92–S120
30. Groves L., Shellenberger M.K., Davis C.S. Tizanidine treatment of spasticity: a meta–analysis of controlled, double–blind, comparative studies with baclofen and diazepam. //Adv. Ther. –1998. –Vol.15, N.4. –P.241–251
31. Hassan N., McLellan D.L. Double–blind comparison of single doses of DS103–282, baclofen and placebo for suppression of spasticity. //J. Neurol. Neurosurg. Psychiatry. –1980. –Vol.43, N.12. –P.1132–1136
32. Jentsch J.D., Taylor J.R. Impulsivity resulting from frontostriatal dysfunction in drug abuse: implications for the control of behavior by reward–related stimuli. //Psychopharmacol. –1999. –Vol.146. –P.373–390
33. Joseph F.G., Scolding N.J. Cerebral vasculitis: a practical approach. //Pract. Neurol. –2002. –Vol.2. –P.80–93
34. Mayer N.H. Spasticity and the stretch reflex. //Muscle & Nerve. –1997. –Vol.20, Suppl.6. –P.S1–S13
35. Miettinen T.J., Kanto J.H., Salonen M.A., Scheinin M. The sedative and sympatholytic effects of oral tizanidine in healthy volunteers. //Anesth. Analg. –1996. –Vol.82, N.4. –P.817–820
36. Moore P.M., Richardson B. Neurology of the vasculitides and connective tissue diseases. //J. Neurol. Neurosurg. Psychiatry. –1998. –Vol.65. –P.10–22
37. Nance P.W., Sheremata W.A., Lynch S.G. et al. Relationship of the antispasticity effect of tizanidine to plasma concentration in patients with multiple sclerosis. //Arch. Neurol. –1997. –Vol.54, N.6. –P.731–736
38. Siva A. Vasculitis of the nervous system. //J. Neurol. –2001. –Vol.248. –P.451–468
39. Stein R., Nordal H.J., Oftedal S.I., Slettebo M. The treatment of spasticity in multiple sclerosis: a double–blind clinical trial of a new anti–spastic drug tizanidine compared with baclofen. //Acta Neurol. Scand. –1987. –Vol.75, N.3. –P.190–194
40. Verdejo–Garcia A., Lopez–Torrecillas F., Gimenez C.O., Perez–Garcia M. Clinical implications and methodological challenges in the study of the neuropsychological correlates of cannabis, stimulant, and opioid abuse. //Neuropsychol. Rev. –2004. –Vol.14, N.1. –P.1–41
41. Wagstaff A. J., Bryson H.M. Tizanidine. A review of its pharmacology, clinical efficacy and tolerability in the management of spasticity associated with cerebral and spinal disorders. //Drugs. –1997. –Vol.53, N.3. –P.435–452
42. Wiesendanger M. Neurobiology of spasticity. //In: Spasticity: The current status of research and treatment. Ed. by M.Emre, R.Benecke. –Carnforth etc.: The Parthenon Publishing Group, 1989. –P.45–61
43. Wiesendanger M., Palmeri A., Corboz M. Some pathophysiological considerations about muscle tone and spasticity. //In: The origin and treatment of spasticity. Ed. by R.Benecke et al. –Carnforth etc.: The Parthenon Publishing Group, 1990. –P.15–27
44. Winkler P.A. Assessment tools in the management of spasticity: Perspective from physical therapy. /In: Physiology and Management of Spasticity. Ed. C.O’Brien. –Deerfield: Discovery International, 1996. –P.3–14
45. Yatsu F.M., Grotta J.C., Pettigrew L.C. Stroke: 100 Maxims. –St. Louis etc.: Mosby, 1995
46. Young R.R. Spasticity: a review. //Neurology. –1994. –Vol.44 (Supp.9). –P.S12–S20
Парфенов В.А.
Московская медицинская академия им. И.М. Сеченова
Актуальность проблемы
В России ежегодно регистрируется 300-400 тысяч инсультов, что приводит к наличию более одного миллиона больных, перенесших инсульт. Более чем у половины из них остаются двигательные нарушения, вследствие которых существенно снижается качество жизни и нередко развивается стойкая инвалидность (1).
Двигательные нарушения после перенесенного инсульта чаще всего проявляются гемипарезом или монопарезом конечности с повышением мышечного тонуса по типу спастичности (1,2,9). У больных инсультом спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, сравнительно редко (чаще всего при восстановлении двигательных) функций наблюдается спонтанное уменьшение спастичности. Во многих случаях у больных инсультом спастичность ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами (2,5,6,9,14).
Восстановление утраченных двигательных функций максимально в течение двух-трёх месяцев с момента инсульта, в дальнейшем темпы восстановления снижаются значительно. Через год после развития инсульта мало вероятно уменьшение степени пареза, однако возможно улучшение двигательных функций и уменьшение инвалидности путём тренировки равновесия и ходьбы, использования специальных приспособлений для передвижения и снижения спастичности в паретичных конечностях (1,2,6,9,14)
Основная цель лечения постинсультной спастичности состоит в улучшении функциональных возможностей паретичных конечностей, ходьбы, самообслуживания больных. К сожалению, в значительной части случаев возможности лечения спастичности ограничиваются только уменьшением боли и дискомфорта, связанного с высоким мышечным тонусом, облегчением ухода за парализованным пациентом или устранением имеющегося косметического дефекта, вызванного спастичностью (2,6,14).
Один из наиболее важных вопросов, который приходится решать при ведении больного с постинсультной спастичностью сводится к следующему: ухудшает или нет спастичность функциональные возможности больного? В целом, функциональные возможности конечности у больного с постинсультным парезом конечности хуже при наличии выраженной спастичности, чем при её лёгкой степени. Вместе с тем у части больных при выраженной степени пареза спастичность в мышцах ноги может облегчать стояние и ходьбу, а её снижение привести к ухудшению двигательной функции и даже к падениям (2,6,14).
Перед тем, как начать лечить постинсультную спастичность, необходимо определить возможности лечения у конкретного больного (улучшение двигательных функций, уменьшение болезненных спазмов, облегчение ухода за пациентом и др.) и обсудить их с больным и (или) его родственниками. Возможности лечения во многом определяются сроками с момента заболевания и степенью пареза, наличием когнитивных расстройств (2,6,14). Чем меньше сроки с момента развития инсульта, вызвавшего спастический парез, тем более вероятно улучшение от лечения спастичности, потому что оно может привести к существенному улучшению двигательных функций, предотвратив формирование контрактур и повысив эффективность реабилитации в период максимальной пластичности центральной нервной системы. При длительном сроке заболевания менее вероятно существенное улучшение двигательных функций, однако можно значительно облегчить уход за больным и снять дискомфорт, вызванный спастичностью. Чем меньше степень пареза в конечности, тем более вероятно, что лечение спастичности улучшит двигательные функции (14).
Лечебная гимнастика
Лечебная гимнастика представляет наиболее эффективное направление ведения больного с постинсультным спастическим гемипарезом, она направлена на тренировку движений в паретичных конечностях и предотвращение контрактур (2,14).
В качестве методов физиотерапии используются лечение положением, обучение пациентов стоянию, сидению, ходьбе (с помощью дополнительных средств и самостоятельно), бинтование конечности, применение ортопедических аппаратов, тепловые воздействия на спастичные мышцы, а также электрическая стимуляция определенных мышечных групп, например разгибателей пальцев кисти или передней большеберцовой мышцы (4).
Больным, имеющим выраженную спастичность в сгибателях верхних конечностей, не следует рекомендовать интенсивные упражнения, которые могут значительно усилить мышечный тонус, например, сжимание резинового кольца или мяча, использование экспандера для развития сгибательных движений в локтевом суставе.
Массаж мышц паретичных конечностей, имеющих высокий мышечный тонус, возможен только в виде легкого поглаживания, напротив, в мышцах антогонистах, можно использовать растирание и неглубокое разминание в более быстром темпе.
Иглорефлексотерапия относительно часто используется в нашей стране в комплексной терапии больных, имеющих постинсультный спастический гемипарез, однако контролируемые исследования, проведенные за рубежом, не показывают существенной эффективности этого метода лечения (10).
Миорелаксанты
В качестве лекарственных средств, принимаемых внутрь для лечения постинсультной спастичности, в клинической практике используются преимущественно баклофен и тизанидин (5-7). Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры и вследствие этого предупредить развитие контрактур. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты (2,5-7,14). Лечение миорелаксантами начинают с минимальной дозы, затем её медленно повышают для достижения эффекта. Антиспастические средства обычно не комбинируют.
Баклофен (Баклосан) оказывает антиспастическое действие преимущественно на спинальном уровне.
Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК); он связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделению возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности.
За свою долгую историю остается препаратом выбора в лечении спастичности спинального и церебрального происхождения.
Баклофен оказывает также центральное анальгезирующее действие и оказывает противотревожный эффект. Он хорошо всасывается из желудочно-кишечного тракта, максимальная концентрация в крови достигается через 2-3 часа после приёма. Баклофен (баклосан) используется при спинальной (спинальная травма, рассеянный склероз) и церебральной спастичности; он эффективен при болезненных мышечных спазмах различного генеза. Баклофен (Баклосан) Начальная доза составляет 5-15 мг в сутки (в один или три приёма), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта, препарат принимают во время еды. Максимальная доза баклофена (баклосана) для взрослых составляет 60-75 мг в сутки. Побочные эффекты проявляются сонливостью, головокружением в начале лечения, хотя они имеют четко дозозависимый характер и в дальнейшем могут ослабевать. Иногда возникают тошнота, запор, диарея, артериальная гипотония.
Баклофен можно использоваться интратекально с помощью специальной помпы при спастичности, вызванной различными неврологическими заболеваниями, включая последствия инсульта (8,11,13). Использование баклофеновой помпы в сочетании с лечебной гимнастикой, физиотерапией может улучшить скорость и качество ходьбы у больных с постинсультной спастичностью, способных к самостоятельному передвижению (8). Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств (13). Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт (11). Тизанидин – миорелаксант центрального действия, агонист альфа-2 адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Препарат обладает также умеренным центральным анальгезирующим действием, эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах. Начальная доза препарата составляет 2-6 мг в сутки в один или три приёма, средняя терапевтическая доза – 12-24 мг в сутки, максимальная доза – 36 мг в сутки. В качестве побочных эффектов могут отмечаться выраженная сонливость, сухость во рту, головокружение и незначительное снижение артериального давления.
Ботулинический токсин
У больных, перенесших инсульт и имеющих локальную спастичность в паретичных мышцах, можно использовать ботулинический токсин типа А или ботулотоксин (ботокс, диспорт). Использование ботулинического токсина показано, если у больного, перенесшего инсульт, имеется мышца с повышенным тонусом без контрактуры, а также отмечаются боль, мышечные спазмы, снижение объёма движений и нарушение двигательной функции, связанные со спастичностью этой мышцы (2-4,12,14). Действие ботулинического токсина при внутримышечном введении вызвано блокированием нервно-мышечной передачи, обусловленным подавлением высвобождения нейромедиатора ацетилхолина в синаптическую щель.
Клинический эффект после инъекции ботулинического токсина отмечается спустя несколько дней и сохраняется в течение 2-6 месяцев, после чего может потребоваться повторная инъекция. Лучшие результаты отмечаются при использовании ботулинического токсина в ранние сроки (до года) с момента заболевания и легкой степени пареза конечности. Применение ботулинического токсина может быть особенно эффективно в тех случаях, когда имеется эквино-варусная деформация стопы, вызванная спастичностью задней группы мышц голени, или высокий тонус мышц сгибателей запястья и пальцев, ухудшающий двигательную функцию паретичной руки (14). В контролированных исследованиях доказана эффективность диспорта при лечении постинсультной спастичности в руке (3).
В качестве побочных эффектов от использования ботулотоксина могут быть кожные изменения и боли в месте инъекции. Они обычно самостоятельно регрессируют в течение нескольких дней после инъекции. Возможна значительная слабость мышцы, в которую введён ботулотоксин, а также слабость в мышцах, расположенных близко к месту инъекции, локальная вегетативная дисфункция. Однако мышечная слабость обычно компенсируется деятельностью агонистов и не приводит к ослаблению двигательной функции. Повторные инъекции ботулотоксина у части больных дают менее значительный эффект, что связывается с образованием антител к ботулотоксину и блокированием его действия. Ограничение широкого применения ботулинического токсина в клинической практике во многом вызвано его высокой стоимостью.
Хирургические методы лечения
Хирургические операции для уменьшения спастичности возможны на четырёх уровнях - на головном мозге, спинном мозге, периферических нервах и мышцах (2,14). У больных с постинсультной спастичностью они используются редко. Эти методы чаще применяются при детском церебральном параличе и спинальной спастичности, вызванной спинальной травмой.
Хирургические операции на головном мозге включают электрокоагуляцию бледного шара, вентролатерального ядра таламуса или мозжечка и имплантацию стимулятора на поверхность мозжечка. Эти операции используются редко и имеют определённый риск осложнений.
На спинном мозге может быть проведено продольное рассечение конуса (продольная миелотомия) с целью разрыва рефлекторной дуги между передними и задними рогами спинного мозга. Операция применяется при спастичности нижних конечностей, она технически сложна и связана с высоким риском осложнений, поэтому используется редко. Шейная задняя ризотомия может привести к снижению спастичности не только в верхних конечностях, но и в нижних, однако выполняется редко из-за риска осложнений. Селективная задняя ризотомия представляет наиболее частое вмешательства среди операций на спинном мозге и его корешках, она обычно используется при спастичности в нижних конечностях на уровне от второго поясничного до второго крестцового корешка.
Рассечение периферических нервов может устранить спастичность, однако эта операция нередко осложняется развитием болей, дизестезий и нередко требует дополнительной ортопедической операции, поэтому используется редко.
Значительная часть хирургических операций у пациентов со спастичностью различного генеза проводится на мышцах или их сухожилиях. Удлинение сухожилия мышцы или перемещение мышцы уменьшает активность интрафузальных мышечных волокон, снижая тем самым спастичность. Эффект от операции сложно прогнозировать, иногда требуется несколько операций. При развитии контрактуры хирургическое вмешательство на мышцах или их сухожилиях нередко представляет единственный метод лечения спастичности.
Заключение
Лечение постинсультной спастичности представляет актуальную проблему современной неврологии. Ведущую роль в лечении постинсультной спастичности имеет лечебная гимнастика, которая должна начинаться уже с первых дней развития инсульта и быть направлена на тренировку утраченных движений, самостоятельное стояние и ходьбу, а также профилактику развития контрактур в паретичных конечностей.
В тех случаях, когда у больного с постинсультным парезом конечности имеется локальная спастичность, вызывающая ухудшение двигательных функций, можно использовать локальное введение препаратов ботулинического токсина.
В качестве лекарственных антиспастических средств, применяемых внутрь, рекомендуются Баклофен (Баклосан)
и тизанидин, которые способны уменьшить повышенный тонус, облегчить физиотерапевтические занятия, а также уход за парализованным больным. Одним из перспективных методов лечения посинсультной спастичности является введение баклофена интратекально с помощью специальной помпы, эффективность которого активно изучается в последние годы.
ЛИТЕРАТУРА
1. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. В кн.: Болезни нервной системы. Руководство для врачей. Под ред. Н.Н. Яхно. М.: Медицина, 2005, Т.1., С. 232-303.
2. Парфенов В.А.. Спастичность В кн.: Применение ботокса (токсина ботулизма типа А) в клинической практике: руководство для врачей / Под ред. О.Р. Орловой, Н.Н. Яхно. – М.: Каталог, 2001 – С. 91-122.
3. Bakheit A.M., Thilmann A.F., Ward A.B. et al. A randomized, double-blind, placebo-controlled, dose-ranging study to compare the efficacy and safety of three doses of botulinum toxin type A (Dysport) with placebo in upper limb spasticity after stroke // Stroke. – 2000. – Vol. 31. – P. 2402-2406.
4. Bayram S., Sivrioglu K., Karli N. Et al. Low-dose botulinum toxin with short-term electrical stimulation in poststroke spastic drop foot: a preliminary study // Am J Phys Med Rehabil. – 2006. - Vol. 85. – P. 75-81.
5. Chou R., Peterson K., Helfand M. Comparative efficacy and safety of skeletal muscle relaxants for spasticity and musculoskeletal conditions: a systematic review. // J Pain Symptom Manage. – 2004. – Vol. 28. – P.140–175.
6. Gallichio J.E. Pharmacologic management of spasticity following stroke. // Phys Ther 2004. – Vol. 84. – P. 973–981.
7. Gelber D. A., Good D. C., Dromerick A. et al. Open-Label Dose-Titration Safety and Efficacy Study of Tizanidine Hydrochloride in the Treatment of Spasticity Associated With Chronic Stroke // Stroke. – 2001. - Vol.32. – P. 1841-1846.
8. Francisco G.F., Boake C. Improvement in walking speed in poststroke spastic hemiplegia after intrathecal baclofen therapy: a preliminary study // Arch Phys Med Rehabil. – 2003. – Vol. 84. – P. 1194-1199.
9. Formisano R., Pantano P., Buzzi M.G. et al. Late motor recovery is influenced by muscle tone changes after stroke // Arch Phys Med Rehabil. – 2005. – Vol. 86. – P.308-311.
10. Fink M., Rollnik J.D., Bijak M. Et al. Needle acupuncture in chronic poststroke leg spasticity // Arch Phys Med Rehabil. - 2004. – Vol. 85. – P.667-672.
11. Ivanhoe C.B., Francisco G.E., McGuire J.R. et al. Intrathecal baclofen management of poststroke spastic hypertonia: implications for function and quality of life // Arch Phys Med Rehabil. – 2006. – Vol. 87. – P. 1509-1515.
12. Ozcakir S., Sivrioglu K. Botulinum toxin in poststroke spasticity // Clin Med Res. – 2007. – Vol. 5. – P.132-138.
13. Taira T., Hori T. Intrathecal baclofen in the treatment of post-stroke central pain, dystonia, and persistent vegetative state // Acta Neurochir Suppl. – 2007. – Vol.97. – P. 227-229.
14. Ward A.B. A summary of spasticity management – a treatment algorithm // Eur. J. Neurol. – 2002. – Vol. 9. – Suppl.1. – P. 48-52.
Спастика мышц после инсульта ― это повышение мышечного тонуса, которое существенно снижает качество жизни.
Сокращение мускулатуры как импульс на растяжение происходит на фоне моно- или гемипареза (односторонняя и двухсторонняя парализации соответственно).
Причиной подобных процессов является поражение клеток двигательных путей мозга. Постинсультной спастичности подвержены такие участки:
При длительном пребывании в лежачем положении симптоматика постепенно нарастает.
Положительная тенденция наблюдается при восстановлении двигательных функций, которое достигается разными методами.
Спастика после инсульта:
лечение лекарственными препаратами
Успешность терапии напрямую зависит от времени, прошедшего с момента заболевания.
Чем раньше начать лечение, тем положительнее прогнозы на выздоровление. Наилучшего результата можно достичь при начале восстановления в первые месяцы после удара, но не позднее, чем через год.
Для обездвиживания группы мышц за счет блокирования нейронной передачи практикуют введения ботулотоксинов («Диспорт», «Ксеомин», «Ботокс»). Эффект сохраняется в среднем полгода, после чего может потребоваться повторное введение препаратов ботулотоксического ряда.
Баклофеновая помпа используется интраректально. Действует на спинальном уровне благодаря снижению количества производства ряда аминокислот (аспартат, глутамат).
Кроме снятия спастичности, миорелаксант центрального действия помогает добиться значительных успехов в уменьшении дистонических расстройств, а также минимизации болевых ощущений.
Схема приема предполагает планомерное увеличение дозировки от 15 до 60 мг в сутки.
Спастика руки после инсульта устраняется с помощью создания эффекта бани.
Конечность помещается в мешок с листьями березы, который фиксируют и оставляют на ночь. Аналогично работают и со спастичностью в ногах, при условии, что размеры емкости соответствуют длине конечности до поясницы.
Лечение спастики после инсульта иглоукалыванием
Иглорефлексотерапия является популярным методом лечения в постсоветских странах, но клинические исследования, проведенные за рубежом, не подтверждают эффективность такой методики.
Упражнения от спастики после инсульта
Это самый эффективный способ борьбы с таким неприятным последствием. Нагрузки не должны быть слишком изнуряющими, поскольку чрезмерная интенсивность только ухудшает состояние больного (увеличивается тонус).